Вторая теорема шеннона. Теорема Шеннона и передача информации
Определение: Термодинамика - наука о закономерностях превращения энергии .
В термодинамике широко используется понятие термодинамической системы .
Определение: термодинамической системой называется совокупность материальных тел, взаимодействующих, как между собой, так и с окружающей средой . Все тела находящиеся за пределами границ рассматриваемой системы называются окружающей средой .
Поскольку одно и тоже тело, одно и тоже вещество при разных условиях может находиться в разных состояниях, (пример: ледvводаvпар, одно вещество при разной температуре) вводятся, для удобства, характеристики состояния вещества - так называемые параметры состояния .
Перечислим основные параметры состояния вещества:
Температура тел - определяет направление возможного самопроизвольного перехода тепла между телами .
В настоящее время в мире существует несколько температурных шкал и единиц измерения температуры. Наиболее распространенная в Европе шкала Цельсия где нулевая температура v температура замерзания воды при атмосферном давлении, а температура кипения воды при атмосферном давлении принята за 100 градусов Цельсия (ºС). В Северной Америке используется шкала Фаренгейта. Для термодинамических расчетов очень удобна абсолютная шкала или шкала Кельвина. За ноль в этой шкале принята температура абсолютного нуля, при этой температуре прекращается всякое тепловое движение в веществе. Численно один градус шкалы Кельвина равен одному градусу шкалы Цельсия.
Температура, выраженная по абсолютной шкале, называется абсолютной температурой .
Соотношение для перехода от градусов Цельсия к градусам Кельвина:
T [K] = t [º C] + 273.15
T-температура в Кельвинах;
t v температура в градусах Цельсия.
Давление - представляет собой силу, действующею по нормали к поверхности тела и отнесенную к единице площади этой поверхности .
Для измерения давления применяются различные единицы измерения. В стандартной системе измерения СИ единицей служит Паскаль (Па).
Соотношение между единицами:
1 бар = 10 5 Па
1 кг/см 2 (атмосфера) = 9.806710 4 Па
1мм рт. ст (миллиметр ртутного столба) = 133 Па
1 мм вод. ст. (миллиметр водного столба) = 9.8067 Па
Плотность - отношение массы вещества к объему занимаемому эти веществом .
Удельный объем - величина обратная плотности т.е. отношения объема занятого веществом к его массе .
![]()
Определение: Если в термодинамической системе меняется хотя бы один из параметров любого входящего в систему тела, то в системе происходит термодинамический процесс .
Основные термодинамические параметры состояния Р, V, Т однородного тела зависят один от другого и взаимно связаны уравнением состояния:
Для идеального газа уравнение состояния записывается в виде:
P - давление
v - удельный объем
T - температура
R - газовая постоянная (у каждого газа свое значение)
Если известно уравнение состояния, то для определения состояния простейших систем достаточно знать две независимые переменные из 3-х
Р = f1 (v, т); v = f2 (Р, Т); Т = f3 (v, Р)
Термодинамические процессы часто изображаются на графиках состояния, где по осям отложены параметры состояния. Точки, на плоскости такого графика, соответствуют определенному состоянию системы, линии на графике соответствуют термодинамическим процессам, переводящим систему из одного состояния в другое.
Рассмотрим термодинамическую систему, состоящую из одного тела v какого либо газа в сосуде с поршнем, причем сосуд и поршень в данном случае является внешней средой. Пусть, для примера, происходит нагрев газа в сосуде, возможны два случая:
1) Если поршень зафиксирован и объем не меняется, то произойдет повышение давления в сосуде. Такой процесс называется изохорным (v=const), идущий при постоянном объеме;
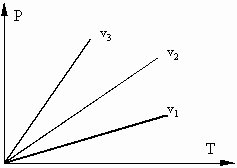
Изохорные процессы в P - T координатах:
v 1 >v 2 >v 3
2) Если поршень свободен, то нагреваемый газ будет расширяться, при постоянном давлении такой процесс называется изобарическим (P=const), идущим при постоянном давлении.
Изобарные процессы в v - T координатах
P 1 >P 2 >P 3

Если, перемещая поршень, изменять объем газа в сосуде то, температура газа тоже будет изменяться, однако можно охлаждая сосуд при сжатии газа и нагревая при расширении можно достичь того, что температура будет постоянной при изменениях объема и давления, такой процесс называется изотермическим (Т=const).
Изотермические процессы в P-v координатах

Процесс, при котором отсутствует теплообмен между системой и окружающей средой, называется адиабатным , при этом количество теплоты в системе остается постоянными (Q=const). В реальной жизни адиабатных процессов не существует поскольку полностью изолировать систему от окружающей среды не возможно. Однако часто происходят процессы, при которых теплообменном с окружающей средой очень мал, например, быстрое сжатие газа в сосуде поршнем, когда тепло не успевает отводиться за счет нагрева поршня и сосуда.
Примерный график адиабатного процесса в P - v координатах

Определение: Круговой процесс (Цикл) - это совокупность процессов, возвращающих систему в первоначальное состояние . Число отдельных процессов может быть любым в цикле.
Понятие кругового процесса является для нас ключевым в термодинамике, поскольку работа АЭС основана на паро-водяном цикле, другими словами мы можем рассматривать испарение воды а активной зоне (АЗ), вращение паром ротора турбины, конденсацию пара и поступление воды в АЗ как некий замкнутый термодинамический процесс или цикл.
Теплота и работа .
Тела, участвующие в процессе, обмениваются между собой энергией. Энергия одних тел увеличивается, других - уменьшается. Передача энергии от одного тела к другому происходит 2-мя способами:
Первый способ передачи энергии при непосредственном контакте тел, имеющих различную температуру, путем обмена кинетической энергии между молекулами соприкасающихся тел (или лучистым переносом при помощи электромагнитных волн).
Энергия передается от более нагретого тела к менее нагретому.
Энергия кинетического движения молекул называется тепловой, поэтому такой способ передачи энергии называется передача энергии в форме теплоты. Количество энергии, полученной телом в форме теплоты, называется подведенной теплотой (сообщенной), а количество энергии, отданное телом в форме теплоты - отведенной теплотой (отнятой).
Обычное обозначение теплоты Q, размерность Дж. В практических расчетах важное значение приобретает отношение теплоты к массе - удельная теплота обозначается q размерность Дж/кг.
Подведенная теплота - положительна, отведенная - отрицательна.
Второй способ передачи энергии связан с наличием силовых полей или внешнего давления. Для передачи энергии этим способом тело должно либо передвигаться в силовом поле, либо изменять свой объем под действием внешнего давления.
Этот способ называется передачей энергии в форме работы .
Если в качестве примера тела рассматривать газ в сосуде с поршнем то в случае приложения внешней силы к поршню происходит сжатие газа - работа совершается над телом, а в случае расширения газа в сосуде работу, перемещение поршня, совершает само тело (газ).
Количество энергии, полученное телом в форме работы называется совершенной над телом работой, а отданная - затраченной телом работой .
Количество энергии в форме работы обычно обозначается L размерность Дж. Удельная работа - отношение работы к массе тела обозначается l размерность - Дж/кг.
Определение: Рабочие тело - определенное количество вещества, которое, участвуя в термодинамическом цикле, совершает полезную работу .
Рабочим телом в реакторной установке РБМК является вода, которая после испарения в активной зоне в виде пара совершает работу в турбине, вращая ротор.
Определение: Передача энергии в термодинамическом процессе от одного тела к другому, связанная с изменением объема рабочего тела, с перемещением его во внешнем пространстве или с изменением его положения называется работой процесса .
Что такое термодинамика
Определение
Термодинамика -- важнейшая часть физики. Ее выводы используются в гиро- и аэродинамике, оптике, физической химии многих других науках и прикладных разработках.
Возникла термодинамика в начале XIX века. В то время начала свое развитие теплотехника. Термодинамика стала ее теоретической основой. Ее целью в то время было изучение закономерностей, которые определяют процессы превращения тепла в механическую работу с помощью тепловых двигателей и поиск условий, при которых максимальна эффективность таких превращений. Основы термодинамики заложил в своих работах Саади Карно, французский инженер и физик, который и исследовал тепловые двигатели. Тогда еще теплота рассматривалась как некоторое вещество -- теплород, которое не имеет массы и не может быть создано или уничтожено. Впоследствии термодинамика вышла за границы узкой технической задачи. Основным содержанием современной термодинамики стало изучение законов тепловой формы движения материи и связанных с этим явлений.
Какие процессы изучает термодинамика
Термодинамика изучает макроскопические процессы, которые происходят в телах, системах тел. Эта наука не использует специальных гипотез и представлений о строении вещества. Не задает вопросы о природе теплоты. Выводы термодинамики основаны на общих принципах (началах), которые получены обобщением эмпирических данных.
Термодинамика изучает только термодинамически равновесные состояния систем или очень медленные процессы, которые могут быть представлены совокупностью равновесных. Эта наука также изучает законы перехода от одного равновесного состояния к другому.
Выводы термодинамики весьма общие, так как получают их без использования упрощенных моделей. Термодинамика многие уравнения берет из опыта, или молекулярно -- кинетической теории. Но здесь необходимо отметить, что практика показала, что аксиомы термодинамики имеют границы применимости. Так классическая термодинамика плохо применима в системах с малыми размерами, так как не рассматривает флуктуации состояния, которые в микромире имеют существенное значение.
Итак, основную идею термодинамики определим так:
Основная идея термодинамики
Макроскопические системы состоят из большого количества частиц. Состояния системы характеризуются вполне конкретными параметрами. Каждая система подчиняется закону сохранения энергии.
В термодинамике закон сохранения энергии формулируется как начала термодинамики. Поведение макросистемы описывается исходя из начал термодинамики. В термодинамике сформулированы три начала. Первое начало -- следствие закона сохранения энергии:
Первое начало термодинамики
\[\delta Q=dU+\delta A\ \left(1\right),\]
где $\delta Q$- элемент тепла (или бесконечно малое количество) подводимое к термодинамической системе. Изучение движение и превращений этой формы энергии является предметом термодинамики, $dU$- изменение внутренней энергии системы, $\delta A$ -- элементарная работа. Бесконечно малые величины здесь обозначены разными символами (d и $\delta $), это сделано намерено. С целью подчеркнуть, что свойства этих малых величин различны. Первое начало термодинамики не дает понятия о направлении прохождения процесса. Поэтому необходимо второе начало. Именно оно характеризует направление процессов в термодинамике. Существую несколько формулировок второго начала термодинамики. По форме они отличаются, но по смыслу он эквивалентны. Приведем одну из формулировок, ее дал Томпсон (лорд Кельвин):
Второе начало термодинамики
«Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет уменьшения внутренней энергии теплового резервуара».
Третье накладывает ограничение на процессы. Его сформулируем:
Третье начало термодинамики
«Абсолютный нуль недостижим посредством конечного числа операций».
Математическим аппаратом термодинамики является теория дифференциальных форм и уравнения в частных производных.
Задание: Идеальный одноатомный газ совершает циклический процесс (рис.1).
Определите КПД цикла, если известны $V_1,\ V_2,$ $p_1,\ p_2$.
Кпд ($\eta $) цикла в данном случае удобно определить как:
\[\eta =\frac{A}{Q^+}\left(1.1\right),\]
где A -- работа газа в круговом процессе, $Q^+$- количество теплоты, подведенное газу от нагревателя.
Круговой процесс (цикл), который изображен на рис.1, состоит из четырех последовательных процессов. Определим, в каких процессах тепло подводится. Очевидно, что это процессы AB и BC.
Процесс AB -- изобарный. Запишем первое начало термодинамики и найдем количество теплоты, пущенное газом в этом процессе.
\[\triangle Q=\triangle U+A\ \left(1.2\right).\]
Работа в изобарном процессе может быть найдена как:
Следовательно, для процесса AB мы получим:
Изменение внутренней энергии газа в процессе AB, имеет формулу:
\[\triangle U_{AB}=\frac{i}{2}\nu R\left(T_2-T_1\right)\left(1.5\right).\]
Для того, чтобы найти $\left(T_2-T_1\right)$, используем уравнение Менделеева - Клайперона для идеального газа. Запишем его для двух состояний (точек A и B):
\ \
Найдем разность (1.7) и (1.6), получим:
Подставим (1.8) в (1.5), получим:
\[\triangle U_{AB}=\frac{i}{2}p_1\left(V_2-V_1\right)\left(1.9\right).\]
Следовательно, количество теплоты, полученное газом в процессе AB равно:
\[\triangle Q_{AB}=p_1\left(V_2-V_1\right)+\frac{i}{2}p_1\left(V_2-V_1\right)\ (1.10).\]
Теперь рассмотрим изохорный процесс ВС. Для него количество теплоты, переданное газу равно:
\[\triangle Q_{BC}=\triangle U_{BC\ }\left(1.11\right).\]
так как работа в изохорном процессе равна нулю. Найдем изменений внутренней энергии данного процесса, используя уравнение состояния идеального газа для точек диаграммы B и C:
\ \
Вычтем (1.6) из (1.7), получим:
Подставим (1.14) в (1.11) найдем $\triangle Q_{BC}$:
\[\triangle Q_{BC}=\frac{i}{2}{(p}_2-\ p_1)V_2(1.15).\]
Получим выражение для $Q^+:$
Найдем работу, которую совершает газ в круговом процессе. Она равна из геометрического смысла интегралов площади прямоугольника ABCD, соответственно запишем:
\[\eta =\frac{{(p}_2-\ p_1)\left(V_2-V_1\right)}{{\frac{i}{2}(p}_2V_2-p_1V_1)+p_1{(V}_2-V_1)}\ \left(1.18\right).\]
Ответ: КПД цикла заданного процесса выражается формулой: $\eta =\frac{{(p}_2-\ p_1)\left(V_2-V_1\right)}{{\frac{i}{2}(p}_2V_2-p_1V_1)+p_1{(V}_2-V_1)}$.
Задание: На рис. 2 изображены изотермы AB и CD. Сравните количества теплоты, получаемые газом, в процессах I и II.

Если AB и СВ -- изотермы, изменения внутренней энергии газа процессах I и II одинаковы: \[\triangle U_I=\triangle U_{II}\left(2.1\right).\]
Работа в процессе I равна нулю, так как процесс изохорный, следовательно количество теплоты получаемое газом в процессе I:
\[\triangle Q_I=\triangle U_I\ \left(2.2\right).\]
В процессе II работа газом совершается и она больше 0 ($A_I>0).\ $
\[\triangle Q_{II}=\triangle U_{II}+A=\triangle U_I+A\ \to \triangle Q_{II}>\triangle Q_I\left(2.3\right).\]
Ответ: Количества теплоты получаемое газом в процессе II больше, чем количество теплоты, получаемое газом в процессе I.
Термодинамика - наука, которая изучает тепловые явления, происходящие в телах, не связывая их с молекулярным строением вещества.
В термодинамике считается, что все тепловые процессы в телах характеризуются только лишь макроскопическими параметрами - давлением, объёмом и температурой. А так как их невозможно применить к отдельно взятым молекулам или атомам, то, в отличие от молекулярно-кинетической теории, в термодинамике молекулярное строение вещества в тепловых процессах не учитывается.
Все понятия термодинамики сформулированы как обобщение фактов, наблюдаемых в ходе экспериментов. Из-за этого её называют феноменологической (описательной) теорией тепла.
Термодинамические системы

Термодинамика описывает тепловые процессы, происходящие в макроскопических системах. Такие системы состоят из огромного количества частиц - молекул и атомов, и называются термодинамическими.
Термодинамической системой можно считать любой объект, который можно увидеть невооружённым глазом или с помощью микроскопов, телескопов и других оптических приборов. Главное, чтобы размеры системы в пространстве и время её существования позволяли провести измерения её параметров - температуры, давления, массы, химического состава элементов и др., с помощью приборов, не реагирующих на воздействие отдельных молекул (манометров, термометров и др.).
Для химиков термодинамическкой системой является смесь химических веществ, взаимодействующих между собой в процессе химической реакции. Астрофизики назовут такой системой небесное тело. Смесь горючего с воздухом в автомобильном двигателе, земной шар, наше тело, пишущая ручка, тетрадь, станок и др. - это также термодинамические системы.
Каждая термодинамическая система отделена от окружающей среды границами. Они могут быть реальными - стеклянные стенки пробирки с химическим веществом, корпус цилиндра в двигателе и т.п. А могут быть и условными, когда, например, изучают образование облака в атмосфере.
Если такая система не обменивается с внешней средой ни энергией, ни веществом, то её называют изолированной или замкнутой .
Если же система обменивается с внешней средой энергией, но не обменивается веществом, то она называется закрытой .
Открытая система обменивается с внешней средой и энергией, и веществом.
Термодинамическое равновесие

Это понятие также введено в термодинамику, как обобщение результатов экспериментов.
Термодинамическим равновесием называют такое состояние системы, при котором все её макроскопические величины - температура, давление, объём и энтропия - не изменяются во времени, если система является изолированной. В такое состояние может самопроизвольно перейти любая замкнутая термодинамическая система, если остаются постоянными все внешние параметры.
Самый простой пример системы в состоянии термодинамического равновесия - термос с горячим чаем. Температура в нём одинакова в любой точке жидкости. Хотя термос можно назвать изолированной системой лишь приблизительно.
Любая замкнутая термодинамическая система самопроизвольно стремится перейти в термодинамическое равновесие, если не меняются внешние параметры.
Термодинамический процесс

Если меняется хотя бы один из макроскопических параметров, то говорят, что в системе происходит термодинамический процесс . Такой процесс может возникнуть, если изменяются внешние параметры или система начинает получать или передавать энергию. В результате она переходит в другое состояние.
Вспомним пример с чаем в термосе. Если мы опустим в чай кусочек льда и закроем термос, то сразу же появится разница в температурах в разных частях жидкости. Жидкость в термосе будет стремиться к выравниванию температур. Из областей с более высокой температурой тепло будет передаваться туда, где температура ниже. То есть, будет происходить термодинамический процесс. В конце концов, температура чая в термосе снова станет одинаковой. Но она уже будет отличаться от первоначальной температуры. Состояние системы изменилось, так как изменилась её температура.
Термодинамический процесс происходит, когда ночью остывает песок, нагретый на пляже в жаркий день. К утру его температура понижается. Но как только взойдёт солнце, процесс нагревания начнётся снова.
Внутренняя энергия

Одно из главных понятий термодинамики - внутренняя энергия .
Все макроскопические тела обладают внутренней энергией, которая является суммой кинетических и потенциальных энергий всех частиц (атомов и молекул), из которых состоит тело. Эти частицы взаимодействуют только между собой и не взаимодействуют с частицами окружающей среды. Внутренняя энергия зависит от кинетической и потенциальной энергии частиц и не зависит от положения самого тела.
U = E k +E p
Внутренняя энергия изменяется с изменением температуры. Молекулярно-кинетическая теория объясняет это изменением скорости движения частиц вещества. Если температура тела растёт, то растёт и скорость движения частиц, расстояние между ними становится больше. Следовательно, увеличивается их кинетическая и потенциальная энергия. При понижении температуры происходит обратный процесс.
Для термодинамики важнее не величина внутренней энергии, а её изменение. А изменить внутреннюю энергию можно с помощью процесса теплопередачи или совершая механическую работу.
Изменение внутренней энергии механической работой

Бенджамин Румфорд
Внутреннюю энергию тела можно изменить, совершив над ней механическую работу. Если работа совершается над телом, то механическая энергия превращается во внутреннюю энергию. А если работу совершает тело, то его внутренняя энергия превращается в механическую.
Почти до конца XIX века считалось, что существует невесомое вещество - теплород, которое передаёт тепло от тела к телу. Чем больше теплорода втекает в тело, тем теплее оно будет, и наоборот.
Однако в 1798 г. англо-американский учёный граф Бенджамин Румфорд стал сомневаться в теории теплорода. Причиной тому были нагревания стволов пушек при сверлении. Он предположил, что причиной нагревания является механическая работа, которая совершается во время трения сверла о ствол.
И Румфорд провёл эксперимент. Чтобы увеличить силу трение, взяли тупое сверло, а сам ствол поместили в бочку с водой. К концу третьего часа сверления вода в бочке закипела. Это означало, что ствол получил тепло при совершении механической работы над ним.
Теплопередача

Теплопередачей называют физический процесс передачи тепловой энергии (теплоты) от одного тела к другому либо при непосредственном контакте, либо через разделяющую перегородку. Как правило, теплота передаётся от более тёплого тела к более холодному. Это процесс заканчивается, когда система приходит в состояние термодинамического равновесия.
Энергия, которую получает или отдаёт тело при теплопередаче, называется количеством теплоты .
По способу передачи теплоты теплообмен можно разделить на 3 вида: теплопроводность, конвенция, тепловое излучение.
Теплопроводность

Если между телами или частями тел существует температурная разница, то между ними будет происходить процесс теплопередачи. Теплопроводностью называют процесс переноса внутренней энергии от более нагретого тела (или его части) к менее нагретому телу (или его части).
К примеру, нагрев на огне один конец стального прута, через некоторое время мы почувствуем, что и другой его конец также становится тёплым.
Стеклянную палочку, один конец которой раскалён, мы легко держим за другой конец, не обжигаясь. Но если мы попробуем проделать такой же эксперимент с железным прутом, у нас ничего не получится.
Разные вещества по-разному проводят тепло. Каждое из них имеет свой коэффициент теплопроводности , или удельной проводимости , численно равный количеству теплоты, которая проходит через образец толщиной 1 м, площадью 1 м 2 за 1 секунду. За единицу температуры принимают 1 К.
Лучше всего проводят тепло металлы. Это их свойство мы используем в быту, готовя пищу в металлических кастрюлях или на сковородках. А вот их ручки не должны нагреваться. Поэтому их делают из материалов с плохой теплопроводностью.
Теплопроводность жидкостей меньше. А газы обладают слабой теплопроводностью.
Мех животных также плохо проводит тепло. Благодаря этому они не перегреваются в жаркую погоду и не замерзают в холодную.
Конвенция

При конвенции теплота передаётся струями и потоками газа или жидкости. В твёрдых телах конвенции нет.
Как возникает конвенция в жидкости? Когда мы ставим на огонь чайник с водой, нижний слой жидкости нагревается, его плотность уменьшается, он движется вверх. Его место занимает более холодный слой воды. Через какое-то время он тоже нагреется и тоже поменяется местами с более холодным слоем. И т.д.
Подобный процесс происходит и в газах. Не случайно батареи отопления размещают в нижней части комнаты. Ведь нагретый воздух всегда поднимается в верхнюю часть комнаты. А нижний, холодный, наоборот, опускается. Затем он нагревается также и вновь поднимается, а верхний слой за это время остывает и опускается.
Конвенция бывает естественная и принудительная.
Естественная конвенция постоянно происходит в атмосфере. В результате этого происходят постоянные перемещения тёплых воздушных масс вверх, а холодных - вниз. В результате возникает ветер, облака и другие природные явления.
Когда естественной конвенции недостаточно, применяю принудительную конвенцию. Например, потоки тёплого воздуха перемещают в комнате с помощью лопастей вентилятора.
Тепловое излучение

Солнце нагревает Землю. При этом не происходит ни теплопередачи, ни конвенции. Так почему же тела получают тепло?
Дело в том, что Солнце является источником теплового излучения.
Тепловое излучение - это электромагнитное излучение, возникающее за счёт внутренней энергии тела. Все окружающие нас тела излучают тепловую энергию. Это может быть видимое световое излучение настольной лампы, или источники невидимых ультрафиолетовых, инфракрасных или гамма-лучей.
Но тела не только излучают тепло. Они его также и поглощают. Одни в большей степени, другие в меньшей. Причём тёмные тела и нагреваются, и охлаждаются быстрее, чем светлые. В жаркую погоду мы стараемся надеть светлую одежду, потому что она поглощает меньше тепла, чем одежда тёмных тонов. Автомобиль тёмного цвета нагревается на солнце гораздо быстрее, чем стоящий с ним рядом автомобиль, имеющий светлую окраску.
Это свойство веществ по-разному поглощать и излучать тепло используется при создании систем ночного видения, систем самонаведения ракет на цель и др.
В продолжение нашего курса «Физика для чайников» начнем рассматривать основы такого важнейшего раздела как термодинамика .
Активное развитие термодинамики началось в девятнадцатом веке. Именно тогда люди начали строить первые паровые машины, а потом активно внедрять их в производство. Началась промышленная революция, и, естественно, всем хотелось увеличить коэффициент полезного действия машин, чтобы произвести больше продукции, доехать подальше и в конце-концов получить больше денег. Все это очень хорошо стимулировало развитие науки и наоборот. Но давайте ближе к сути вопроса.

Термодинамика – раздел физики, изучающий макроскопические системы, их наиболее общие свойства, способы передачи и превращения энергии в таких системах.
Что такое макроскопические системы? Это системы, состоящие из очень большого числа частиц. Например, баллон с газом или воздушный шар. Описание таких систем методами классической механики просто невозможно – ведь мы не можем измерить скорость, энергию и другие параметры каждой молекулы газа в отдельности. Тем не менее, поведение всей совокупности частиц подчиняется статистическим закономерностям. По сути любой видимый нами (невооруженным глазом) предмет может быть определен как термодинамическая система.

– реально или мысленно выделяемая макроскопическая физическая система, состоящая из большого числа частиц, не требующая для своего описания привлечения микроскопических характеристик отдельных частиц. Соответственно, для описания термодинамической системы используются макроскопические параметры, не относящиеся к каждой частице, но описывающие систему целиком. Это температура, давление, объем, масса системы и проч.
Важно отметить, что термодинамические системы могут быть замкнутыми и незамкнутыми . Замкнутая система – это такая система, которую при помощи реальной или воображаемой оболочки оградили от окружающей среды, при этом количество частиц в системе остается постоянным.

Система может находится в разных состояниях. Например, мы взяли баллон с газом и начали его нагревать. Тем самым мы изменили энергию молекул газа, они стали двигаться быстрее, и система перешла в какое-то новое состояние с более высокой температурой. Но что будет, если систему оставить в покое? Тогда система через какое-то время придет в состояние термодинамического равновесия .
Что это значит?
Термодинамическое равновесие – это состояние системы, в котором ее макроскопические параметры (температура, объем и др.) остаются неизменными с течением времени.
Термодинамика стоит на трех своих столпах. Существуют три основных постулата или три закона термодинамики. Они называются соответственно первым, вторым и третьим началами термодинамики. Рассмотрим первое начало или первый закон термодинамики.
Первое начало термодинамики
Первое начало термодинамики гласит:
В любой изолированной системе запас энергии остается постоянным.
К слову, у данного постулата есть еще несколько эквивалентных формулировок. Приведем их ниже:
Количество теплоты, полученное системой, идет на изменение внутренней энергии системы, а также на совершение работы против внешних сил.
Невозможен вечный двигатель первого рода (двигатель, совершающий работу без затраты энергии).
Запишем также математическое выражение первого начала термодинамики:
Здесь Q - количество теплоты, дельта U - изменение внутренней энергии, A - работа против внешних сил. Для различных термодинамических процессов в силу их особенностей запись первого начала будет выглядеть по-разному.
Почему невозможен вечный двигатель первого рода?
Людей издревле привлекала ее величество Халява. Философский камень, превращающий любой металл в золото, скатерть самобранка, с которой не нужно готовить, джин, исполняющий любые желания. Еще одной такой идеей была идея вечного двигателя.

Вечный двигатель невозможен, потому что так устроен мир . Об этом говорят нам законы термодинамики. Согласно первому началу термодинамики, количество теплоты, полученное системой, идет на изменение внутренней энергии системы, а также на совершение работы против внешних сил. Например, газ, помещенный в цилиндр с поршнем, получая определенное количество теплоты, увеличивает свою внутреннюю энергию, молекулы движутся быстрее, газ занимает больший объем и толкает поршень (работа против внешних сил). Иными словами, если работа совершается без внешнего притока энергии, она может совершаться лишь за счет внутренней энергии системы, которая рано иди поздно иссякнет, преобразовавшись в совершенную работу, на чем все закончится и система придет к состоянию термодинамического равновесия. Ведь энергия в мире никуда не уходит и не приходит, ее количество остается постоянным, а меняется лишь форма. Конечно, Вы обратили внимание на то, что речь идет о так называемом вечном двигателе первого рода (который может совершать работу без энергии). Спешим заверить, существование вечного двигателя второго рода также невозможно и объясняется вторым началом термодинамики, о котором мы поговорим в ближайшем будущем.

Надеемся, знакомство с термодинамикой прошло для Вас приятно и Вы полюбите ее всем сердцем. Если же этого не произойдет, Вы всегда можете поручить выполнение задач по термодинамике , пока сами занимаетесь более приятными делами.









